Абляция, как метод лечения рака
Современные минимально инвазивные хирургические технологии, характеризующиеся явными и давно доказанными преимуществами, в последнее десятилетие стали значительно шире применяться и в паллиативной медицине.
В настоящее время с паллиативной целью наиболее часто применяются следующие минимально инвазивные хирургические (эндовидеохирургические, эндоскопические) технологии:
- методика чрескожной пункционной эндоскопической гастростомии;
- методика эндоскопического стентирования пищевода и кардии желудка, двенадцатиперстной, толстой кишки;
- методика эндоскопического стентирования желчевыводящих протоков;
- методика эндоскопического лигирования вен пищевода и желудка;
- методика эндоскопического стентирования трахео-бронхиального дерева;
- методика радиочастотной абляции, электрохимического лизиса и необратимой электропорации.
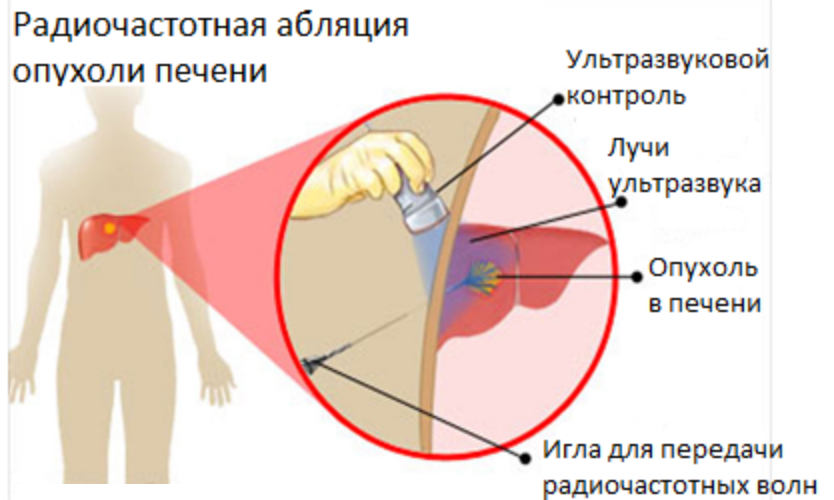
Абляция опухолей печени
После определения показаний к абляции опухоли печени размеров очага новообразования и его границ следует определить доступ, наиболее удобный для проведения процедуры. Для абляции можно использовать как электроды-иглы, так и электроды-спирали. Выполняют лапаротомию, проводят ревизию брюшной полости. Визуально и пальпаторно оценивают расположение опухоли в печени, осматривают брюшину на предмет диссеминации онкопроцесса. После чего проводят ИОУЗИ, в ходе которого уточняется расположение новообразования, его соотношение с сосудисто-секреторными элементами печени, нижней полой веной и желчным пузырем. Далее под его контролем, если новообразование печени недоступно обзору с поверхности печени, или под контролем зрения, если новообразование расположено под капсулой, производят позиционирование электродов в новообразование.
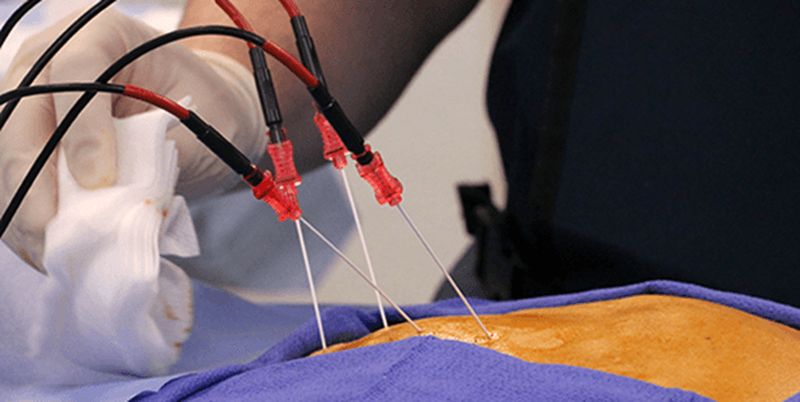
Установка электродов-игл производится вколом их в ткань новообразования, электродов-спиралей – путем их вкручивания. При этом должно отсутствовать напряжение на электроде. После установки электрода начинают процедуру абляции. По мере высушивания тканей произойдет отключение подачи тока на электрод. Такова принципиальная схема работы любого аппарата для выполнения РЧА.
Абляция опухолей легких
Проведение абляции опухолей легких более редкая процедура, нежели абляция опухолей печени. Выполняют торакотомию и, как в случае с опухолями печени, позиционируют электроды в опухоли легкого. Сама процедура абляции и действия персонала при ее выполнении не отличаются от действий при абляции опухоли печени.
Критерии эффективности абляции
Объем зоны абляции оценивается визуально, а также с помощью УЗИ и КТ. Патоморфологически зона абляции является коагуляционным некрозом и визуально представляет собой обугленную ткань черного цвета. При УЗИ определяется гиперэхогенная зона. Гиперэхогенность зоны абляции вызывается образованием пузырьков газа в области гипертермии. Подобное явление может стать препятствием в случаях, когда требуется неоднократное проведение процедуры абляции, так как затруднит ультразвуковой контроль над рабочей частью электрода в зоне проведения процедуры.
В случаях, когда планируется выполнить одномоментную абляцию нескольких новообразований в печени, следует планировать последовательность выполнения процедур и по возможности начинать абляцию с более глубоко расположенных очаговых образований. Восстановление условий для ультразвуковой оценки участка, подвергнувшегося абляции, происходит, как правило, через несколько дней после проведения процедуры абляции.
Оценка эффективности непосредственно после проведения процедуры абляции затруднительна. Применение для этого ультразвуковой доплерографии затруднительно из-за возникновения вышеуказанных артефактов. Решить эту проблему помогает использование ультразвуковых контрастных препаратов. Возможности четкой визуализации кровотока при использовании контрастных веществ помогают оценить эффективность воздействия. Также оценивается скорость кровотока в зоне абляции, что основано на знаниях скорости прохождения контрастного вещества через опухолевую ткань.
При неэффективности процедуры в зоне ее проведения отмечают появление гипоэхогенного ободка и усиление кровотока, что говорит о продолженном росте новообразования. При КТ печени выявляется низко плотная зона, которая не контрастируется ни в артериальную, ни в венозную фазу, что говорит об отсутствии кровотока в ней.
При КТ и МРТ печени можно выделить наиболее постоянные изменения, которые выявляются в зоне проведения абляции: наличие клиновидных участков контрастного усиления в артериальную фазу паренхимы печени, прилежащих к месту рубца, наличие тонкого ободка усиления вокруг зоны абляции. Этот ободок является зоной периферического воспаления с усиленным кровотоком. При проведении чрескожной абляции под контролем КТ отмечается изменение единиц Хаунсфилда в зоне абляции при КТ без контрастного усиления. Так, через 2 мин. отмечается уменьшение этого показателя на 14 ЕД в зоне абляции по сравнению со здоровой паренхимой печени. Через 8 минут разница составляет уже 22 ЕД. Также в зоне, подвергнувшейся абляции, сразу после процедуры могут выявляться пузырьки газа, являющиеся, по-видимому, отображением происходящего в ходе абляции парообразования.
При введении контрастного вещества разница между здоровой паренхимой печени и зоной абляции составляет 55 ЕД. При неправильно выполненной процедуре возможно выявление в зоне абляции контрастируемых участков. В зоне ободка возможно выявление узелка или локального утолщения, или увеличения размеров области, подвергнувшейся абляции. На МРТ в режиме Т2 область абляции выглядит как область с сигналом низкой интенсивности и недостаточным усилением на динамических изображениях.
При ПЭТ область некроза выглядит как зона с отсутствием метаболизма в опухолевой ткани. Кроме того, ПЭТ рассматривают как метод наиболее ранней диагностики рецидивов после проведения абляции. Наиболее ранние изменения, соответствующие локальному рецидиву опухоли, находили через 1 неделю после проведения процедуры абляции, когда в ходе КТ и МРТ не находили изменений. Наиболее информативным с точки зрения онкологии критерием эффективности является биопсия зоны абляции, которая в случае правильно выполненной процедуры не обнаруживает при морфологическом исследовании опухолевых клеток. Правильность выполнения абляции опухолей легких лучше всего контролируется при КТ. Эффективность абляции почек следует оценивать по данным КТ-ангиографии, рентгеновской ангиографии и МРТ.
Так как опухоль почки хорошо васкуляризирована, критерием эффективности абляции является отсутствие кровотока в ней при ангиографии. При КТ-ангиографии критерием эффективности абляции будет служить отсутствие накопления контраста в опухоли. Наиболее достоверным способом оценки эффективности абляции является МРТ. В Т2 режиме область некроза выглядит гипоинтенсивной с гиперинтенсивным ободком, что соответствует зоне кровоизлияния.
Большую диагностическую ценность имеет и УЗИ с доплеровским картированием с контрастным усилением. Эта методика может быть эффективной в отношении богато васкуляризированных опухолей.
Кроме того, имеет значение лабораторная диагностика, направленная на определение уровня онкомаркеров СА 19-9 и РЭА в первые 3 месяца после выполнения абляции. Рост их концентраций может указывать на локальный рецидив.
В многопрофильной международной клинике Медика24 принимают пациентов любой степени тяжести, в том числе с онкологическими диагнозами III и IV стадий. Инкурабельным пациентам наши врачи могут помочь паллиативным лечением, направленным на продление качественной жизни пациента. Паллиативное лечение включает в себя не только уход за пациентом, но и проведение оперативных вмешательств с целью снятия болезненных симптомов. В частности, в клинике проводят: циторедуктивные операции, радиочастотную аблацию метастатического поражения печени и костей, фотодинамическую терапию, стентирование при стенозах внутренних органов, гастростомию, колостомию и др.
Литература
- Введенская Е.С. История развития паллиативной и хосписной помощи больным злокачественными новообразованиями в России // Паллиативная помощь и реабилитация. – 2012. – № 2. С. 55-58.
- Введенская Е.С. О важности принятия рабочего определения паллиативной помощи и ее содержания в преддверии становления служб в регионах // Проблемы стандартизации в здравоохранении. – 2013. – № 1–2. С. 24–29.
- Ганул В.Л., Киркилевский С.И. Рак пищевода: руководство для онкологов и хирургов. – К.: Книга плюс, 2003. – 200 с.
- Гарин A.M., Базин И.С. Злокачественные опухоли пищеварительной системы. М., 2003. – 247 с.
- Контроль симптомов в паллиативной медицине. / Под ред. проф. Г.А. Новикова. – М.: ГЭОТАР-Медиа, 2013. –248 с.
- Концепция развития системы здравоохранения в Российской Федерации до 2020 г., –61 с. – URL: http://www.zdravo2020.ru/concept
Источник: Научно-практический журнал «Паллиативная медицина и реабилитация» № 1. 2018.
Содержание
ПОПУЛЯРНОЕ
- Вскрытие паратонзиллярного абсцесса
- Дренирование желчных протоков при механической желтухе
- Осмотр под лампой Вуда
- Оментэктомия (удаление большого сальника)
- Рассечение девственной плевы
- Эпицистостомия
- Аппендэктомия
- Удаление инородного тела из влагалища
- Установка колостомы
- Химиотерапия при раке с метастазами
